Эндокринный фактор бесплодия
Содержание
Эндокринное бесплодие у женщин (гормональная, секреторная форма): причины, симптомы, лечение, шансы на беременность
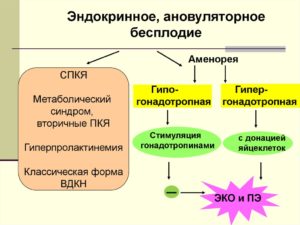
Эндокринное бесплодие обнаруживают у каждой третьей женщины, испытывающей проблемы с зачатием. Это собирательное понятие, оно означает нарушения, кульминацией которых становится отсутствие овуляции.
Начинать лечение эндокринного бесплодия можно только после дифференциального обследования. Врачу нужно установить причину ановуляторных циклов. Не все формы патологии поддаются коррекции.
Если традиционная медицина не помогает, женщине рекомендует вспомогательные репродуктивные технологии.
Симптомы гормонального бесплодия
Гормональное бесплодие проявляется отсутствием беременности при условии регулярной половой жизни без использования контрацептивов. Определить, что проблема имеет именно гормональное происхождение, помогают дополнительные признаки.
Обычно у женщины нарушается менструальный цикл, что сопровождается полным отсутствием менструации или различными нарушениями: затяжными, нестабильными циклами, кровянистыми мажущими выделениями, обильной кровопотерей.
Секреторное бесплодие, сопровождающееся регулярными месячными, обнаружить довольно сложно. Женщина ведет привычный образ жизни, не подозревая о том, что у нее ежемесячная ановуляция на фоне гормональных нарушений. Выделения в данном случае являются менструальноподобным кровотечением, а не настоящей менструацией.
Признаки бесплодия у женщин выражаются в агрессивном течении предменструального синдрома.У девушек незадолго до очередного кровотечения происходит нагрубание молочных желез, из которых может выделяться белесая жидкость, присутствуют выраженные перепады настроения.
Изменение тела по мужскому типу, оволосение, алопеция, угревая сыпь, половой инфантилизм тоже косвенно свидетельствуют об эндокринном бесплодии.
В группу риска входят женщины:
- в возрасте от 25;
- после искусственного прерывания беременности;
- увлекающиеся приемом трав;
- принимающие гормональные средства без назначения врача;
- начавшие раннюю половую жизнь;
- с опухолями половых желез;
- злоупотребляющие алкоголем и наркотиками;
- занимающиеся профессиональным спортом.
Диагностика
Самостоятельно определить гормональные причины бесплодия невозможно. Чтобы выявить проблему, необходимо обратиться к гинекологу. На первом этапе обследования врач задает вопросы о регулярности менструальных циклов, жалобах, перенесенных заболеваниях, наследственных нарушениях и беременностях.
Эта информация нужна, чтобы сориентироваться, какие необходимы обследования. Также во время первого визита выполняется бимануальный осмотр, позволяющий оценить размеры и расположение половых органов, осмотреть шейку матки и взять мазки для определения интимной микрофлоры.
В диагностике эндокринного бесплодия у женщин используются лабораторные, аппаратные и инструментальные методики. После опроса и осмотра специалист назначает УЗИ. Сканирование показывает состояние матки и яичников, дает возможность оценить овариальный резерв и состояние функционального слоя детородного органа.
Анализ на женские гормоны при бесплодии сдается после УЗИ. Важно, чтобы забор крови выполнялся в определенный день цикла, который при нерегулярных кровотечениях помогает установить сканирование. Функции яичников и наличие овуляции позволяют определить: эстрадиол, прогестерон, ФСГ, ЛГ, пролактин, тестостерон, ДГЭАС и гормоны щитовидной железы.
Если выявить причину женского бесплодия не удалось, то пациентке рекомендуется рентген черепа, МРТ, КТ, биопсия функционального слоя матки и лапароскопия.
Основные причины и формы
Спровоцировать секреторное бесплодие могут различные нарушения в работе систем организма: нервной, эндокринной, иммунной, гипоталамо-гипофизарной.
Причинами отсутствия беременности становятся сбои в работе желез внутренней секреции. Нарушения эндокринного генеза могут быть комплексными.
При нарушениях функции одного органа происходит нарушение в другом, в результате чего теряется взаимосвязь и развивается разбалансировка гормонального фона.
Гипоталамо-гипофизарная дисфункция
Взаимосвязь гипоталамуса и гипофиза регулирует работу большинства эндокринных желез. Она не управляет только надпочечниками (мозговой частью) и поджелудочной железой.
Изменение работы гипоталамо-гипофизарной системы происходит при опухолевых процессах или в результате травмы.
Дисфункции предшествует увеличение показателей пролактина, снижающего ФСГ (гормон роста фолликулов) и ЛГ (стимулятора овуляции).
В результате у женщины формируется стойкое гормональное бесплодие, сопровождающееся нарушением менструального цикла или абсолютным отсутствием кровотечений (аменореей).
Недостаточность яичников
Причиной эндокринного бесплодия у женщины становится нарушение функции половых желез. Патология сопровождается снижением количественных показателей эстрадиола, который необходим для роста эндометрия и созревания яйцеклетки. Естественное угнетение функции половых желез происходит с наступлением менопаузы. В остальных случаях говорят о патологическом угасании, которое классифицируется:
- резистентные яичники – железы содержат фолликулы, но не реагирует на выработку гормонов;
- истощенные яичники – железы имеют сниженный овариальный резерв, причиной которого становятся внутренние заболевания или хирургические вмешательства.
СПКЯ
Гормональное бесплодие у женщин нередко бывает спровоцировано синдромом поликистозных яичников.
Заболевание сопровождается патологическими изменениями в строении половых желез, формированием плотной капсулы, снижением чувствительности к инсулину.
Зачастую женщины с СПКЯ имеют длинный менструальный цикл и не подозревают о своем заболевании. У некоторых развивается ожирение, оволосение тела.Следует отличать СПКЯ от мультифолликулярных яичников, при которых овуляция все же происходит и беременность не исключена.
Гиперпролактинемия
Причиной эндокринной формы бесплодия может стать избыточная выработка пролактина – гормона, необходимого для лактации. Избыток данного вещества подавляет секрецию половых гормонов. В результате у женщины тормозятся естественные ежемесячные изменения и формируется бесплодие. Повышение количественных показателей пролактина отмечается у 2-3 женщин из 10.
Мужчины также могут страдать гиперпролактинемией, приводящей к эндокринным нарушениям.
Гиперандрогения
Андрогены – это гормоны, которые в большом количестве присутствуют в мужском организме. У женщины также имеются данные вещества, но в меньшей концентрации. Они обеспечивают половое созревание и поддерживают работу половых желез.
При гиперандрогении возникает избыток гормонов, что приводит к подавлению секреции эстрадиола и прогестерона. Первичная форма патологии обусловлена генетической предрасположенностью. При вторичной андрогены продуцируются надпочечниками из-за формирования опухолей. Заболевание сопровождается нарушением овуляторной функции и изменением женского тела по мужскому типу.
Избыток или дефицит жировых тканей
Эндокринный фактор бесплодия провоцируют изменения массы тела. При резком похудении или наборе подкожно-жировой клетчатки возникает разбалансировка гормонального фона. Если индекс массы тела укладывается в нормальные показатели, то со временем секреторная активность желез восстанавливается самостоятельно.
Дефицит массы тела вызывает снижение показателей половых гормонов, как и ожирение. Шанс на беременность при чрезмерной худобе в два раза ниже, чем при избытке подкожно-жировой клетчатки. Поэтому женщинам, стремящимся к идеальному телу, следует вовремя остановиться.
Нарушение функции щитовидной железы
В организме человека все железы взаимосвязаны, поэтому заболевания щитовидки могут сказаться на работе репродуктивных органов. Для коррекции гормонального фона важно знать, в какую сторону отклоняются показатели гормонов.
При диагностике в эндокринологии и исследовании функции щитовидной железы может обнаружиться гипотиреоз (недостаток гормонов) или гипертиреоз (избыток). Эти состояния приводят к изменению работы яичников, повышению секреции пролактина.
Часто кульминацией патологии становится отсутствие беременности или привычное невынашивание.
Лечение
Лечение эндокринного бесплодия комплексное и длительное. Методики подбираются индивидуально в соответствии с причиной, спровоцировавшей проблему.
Если причиной неудачи становится снижение активности половых желез, то рекомендуется стимуляция гормонами. Эта методика эффективна и обычно приводит к беременности, если нет других преград для зачатия. При повышенной секреции мужских гормонов или пролактина назначается заместительная терапия, подавляющая их концентрацию в организме женщины.
Хирургические методики лечения эндокринного бесплодия приветствуются, если отсутствие беременности вызвано синдромом поликистозных яичников или опухолевыми процессами. В дальнейшем назначаются лечебно-профилактические препараты и гормональные средства.
Диетотерапия способствует решению проблемы гормонального нарушения, вызванного избытком или недостатком подкожно-жировой клетчатки. Во время изменения массы тела у женщин может отмечаться менструальноподобная реакция, вызванная перепадами количественных показателей гормонов.
Нетрадиционные методики коррекции эндокринного фактора обычно не приносят результата. Они могут стать вспомогательным средством, но только по рекомендации врача.
Если принятые меры не принесли результата, то стоит задуматься от методах ЭКО. Возможности современной репродуктивной медицины позволяют подобрать протокол индивидуально, что повышает шансы на успех.
Прогноз
Вероятность успешного лечения эндокринного бесплодия высока. Не менее восьми женщин из десяти успешно беременеют в первый год после проведенной терапии. Легче всего поддается коррекции нарушение работы яичников, гиперадрогения и гиперпролактинемия. Труднее избавиться от бесплодия, вызванного дисфункцией гипоталамо-гипофизарной системы.
Женщина, забеременевшая после лечения эндокринных форм бесплодия, нуждается в постоянном наблюдении. Изменение гормонального фона могут произойти в любой момент.
Поэтому при угрозе прерывания беременности или высокой вероятности преждевременных родов пациентке требуется госпитализация с непрерывным мониторингом за работой эндокринного аппарата и самочувствием будущего ребенка.
У пациенток с такими заболеваниями в анамнезе чаще возникает необходимость использования стимуляторов в силу слабой родовой деятельности.Источник: https://MyZachatie.ru/zhenskie-zabolevaniya/endokrinnoe-besplodie.html
Как развивается эндокринное бесплодие у мужчин и женщин, методы диагностики и лечения

Нарушение работы эндокринных желез может быть причиной как женского, так и мужского бесплодия.
Невозможность женщины забеременеть и выносить ребенка может быть вызвана одним или несколькими из следующих факторов:
- эндокринное бесплодие у женщин, встречающееся у 35-40% пациенток;
- трубное, связанное с непроходимостью маточных труб или со снижением подвижности ресничек, выстилающих трубы изнутри, и наблюдающееся у 20-30% больных;
- заболевания органов женской репродуктивной системы (сальпингоофорит, эндометриоз, миома матки и другие), которые в совокупности обусловливают каждый четвертый случай бесплодия;
- иммунологическое бесплодие, связанное с несовместимостью антигенов матери и отца ребенка или матери и будущего плода (2%);
- необъяснимые случаи длительного отсутствия детей в браке у здоровых родителей (до 15%).
Эндокринный фактор бесплодия – это нарушение овуляции и, соответственно, менструального цикла. Он может быть вызван одной из двух следующих причин:
- ановуляция (отсутствие созревания яйцеклеток в фолликуле);
- недостаточность лютеиновой фазы.
Так же предлагаем прочесть наши статьи о мужском и женском бесплодии (более подробно о видах и причинах).
Ановуляция
Временная ановуляция бывает и у здоровых женщин. В течение года часть циклов являются ановуляторными, и в течение их женщина забеременеть не может. Учащаются случаи ановуляции при тяжелых стрессах, острых инфекционных заболеваниях, резкой перемене климата, под влиянием других неспецифических причин, являющихся необычными для организма.
Постоянная (хроническая) ановуляция свойственная группе заболеваний, при которых нарушается взаимосвязь между основными регулирующими органами – гипоталамусом, гипофизом – и яичниками.
В норме в гипоталамусе ежемесячно вырабатываются гормоны – либерины (их аналогом является, например, гонадотропин-рилизинг фактор), под влиянием которых в гипофизе запускается процесс выработки гонадотропного гормона.
Уже под влиянием последнего в яичниках циклически вырабатываются эстрогены и прогестерон, вызывая пролиферацию эндометрия, а затем его отторжение и менструацию. Под влиянием эстрогенов начинается увеличение фолликула и развитие в нем яйцеклетки, а затем выход ее в брюшную полость – овуляция.
При разбалансировке этой системы на любом уровне в итоге не происходит овуляция и нарушается процесс циклического изменения эндометрия, меняется менструальный цикл.
Ановуляция является причиной примерно трети случаев бесплодия, вызванного эндокринными сдвигами.
Ановуляторные циклы довольно часто похожи на обычные менструальные, длительностью до 36 дней (однако в этом случае более верно говорить «менструальноподобное» кровотечение, потому что полный гормональный цикл не происходит). При нарушении овуляции подобные выделения крови могут быть редкими, скудными, а у части женщин они отсутствуют вообще.
Недостаточность лютеиновой фазы
Недостаточность лютеиновой фазы – изменение деятельности женских желез, отвечающих за ее фертильность — яичников. Оно характеризуется недостаточной выработкой необходимых гормонов, в частности, прогестерона, в желтом теле, образующемся на месте овулировавшей яйцеклетки на поверхности яичника.
Уменьшение синтеза гестагенов желтым телом приводит к снижению секреторного превращения внутреннего слоя матки. В этом случае оплодотворенная яйцеклетка не может закрепиться в маточной стенке и погибает.
Эта ситуация может сопровождаться не только невозможностью зачать ребенка, но и самопроизвольными выкидышами в начале беременности. Именно поэтому для сохранения беременности на ранних сроках назначают препараты прогестерона (Дюфастон, Утрожестан).
Этиология
Причины эндокринного бесплодия нередко кроются в патологических изменениях органов и систем.
1. Болезни гипоталамуса и гипофиза:
- гипоталамический синдром;
- прекращение менструаций при голодании;
- усиление синтеза пролактина;
- повреждение передней доли гипофиза со снижением его эндокринной функции в результате травмы, опухоли и других состояний.
2. Заболевания яичников:
3. Болезни желез внутренней секреции:
- ожирение;
- изменения надпочечников – болезни Иценко-Кушинга, Аддисона;
- адрено-генитальный синдром;
- нарушение обмена гормонов щитовидной железы;
- сахарный диабет.
4. Тяжелые сопутствующие болезни:
- печеночная недостаточность при гепатите или циррозе печени;
- туберкулез;
- разнообразные опухоли;
- ревматологические системные болезни.
5. Наследственная патология:
- синдром Шерешевского-Тернера;
- гермафродитизм в разных формах.
6. Эндометриоз.
7. Гормон-секретирующие опухоли.
Клиническая картина
Симптомы эндокринного бесплодия у женщин включают субъективные проявления (жалобы) и данные объективного и гинекологического осмотра.
Пациенток беспокоят:
- отсутствие беременности;
- задержка менструации до полугода или вообще ее отсутствие (аменорея);
- мажущие выделения между менструальными кровотечениями;
- большой объем кровопотери при менструации, болезненность во время нее;
- выделения слизистого характера из половых путей;
- боли в нижней части живота и поясничной области как в связи с циклом, так и постоянные;
- дискомфорт при половом акте;
- рецидивирующий цистит;
- неприятные ощущения в молочных железах, выделения из сосков;
- увеличение веса, округление и покраснение лица, рост усиков, избыточное оволосение, в том числе по мужскому типу;
- угревая сыпь;
- выпадение волос вплоть до облысения;
- гипертония или «скачки» артериального давления;
- растяжки на боках, животе, бедрах;
- снижение веса;
- предменструальные нарушения.
При расспросе женщины, врач уточняет, когда наступила первая менструация, длительность цикла, объем и болезненность месячных, продолжительность невозможности зачать ребенка, наличие беременностей до настоящего случая, расспрашивает о проводимых гинекологических вмешательствах и их результатах, о применяемых методах предохранения. Уточняется, болела ли пациентка хламидиозом, уреаплазмозом, гонореей и другими инфекциями.
Внешне определяют тип конституции пациентки, формирование вторичных половых признаков, распределение жировых отложений, наличие стрий.
Повышенная секреция андрогенов внешне проявляется угревой сыпью, гирсутизмом, жирной перхотью.
Если определяются багровые широкие растяжки при ожирении живота, груди и тонких конечностях – нужно предположить гиперкортицизм (патологию надпочечников). Тонкие стрии могут быть связаны с гипоталамическим синдромом.
Осматриваются молочные железы, выполняется гинекологическое исследование.
Эндокринное бесплодие

Эндокринное бесплодие, связанное с нарушением овуляции, составляет около 35-40% причин бесплодия.
В основе эндокринного бесплодия при любой патологии имеется нарушение процесса полноценной овуляции. В клинической практике это проявляется ановуляцией (отсутствием овуляции) или неполноценной овуляцией с недостаточной лютеиновой фазой (НЛФ). Эндокринное бесплодие характеризуется целым комплексом симптомов, которые могут проявляться как отдельно, так и в сочетаниях.
Синдром лютеинизации неовулировавшего фолликула
Лютеинизация неовулировавшего фолликула (ЛНФ) является патологией, при которой происходит рост фолликула, его созревание, но овуляции нет. Созревший фолликул при этом лютеинизируется – превращается в ложное желтое тело. Синдром ЛНФ приводит к бесплодию.
Диагностика эндокринных нарушений
Комплексная диагностика эндокринных нарушений включает в себя:
- Изучение данных анамнеза пациента, оценка соматического статуса, гормональный скрининг, который позволяет оценить уровень базальной секреции гормонов в плазме крови в раннюю фолликулиновую фазу менструального цикла (2-3 день от начала менструаций).
- При нарушении менструального цикла по типу олиго-аменореи определяют концетрацию пролактина, гонадотропинов (ФСГ, ЛГ), эстрадиола, тестостерона, дегидроэпиандростерон-сульфата (ДЭА-С), кортизола, тиреотропного гормона, свободных фракций гормонов щитовидной железы: трийодтирозина, тироксина, определяют уровень антител к тиреоидной пероксидазе и тиреоглобулину.
- У пациенток с сохраненным менструальным циклом в раннюю фолликулиновую фазу определяют уровень пролактина, эстрадиола, тестостерона, ДЭА-С, ТТГ ( ТТГ при ЭКО норма должна быть не более 2,5 мЕд/л.), Т3 св., Т4 св., АТ-ТПО, АТ-ТГ.
- Диагноз эндокринного бесплодия может быть поставлен только после оценки овуляции. Оценку активности желтого тела проводят по определению уровня прогестерона и эстрадиола в плазме крови на 6-8 день после овуляции, определенной при УЗ-мониторинге или тестами функциональной диагностики.
Дополнительные методы обследования: УЗИ органов малого таза, УЗИ щитовидной железы, исследование состояния молочных желез, рентгенологическое исследование черепа, биохимическое исследование крови, эндоскопические методы обследования — лапароскопия, гистероскопия.
Тесты на овуляцию
Для оценки гормональной активности яичников и наличия овуляции используют тесты функциональной диагностики: построение графика базальной температуры, мочевой тест на овуляцию и УЗИ-мониторинг созревания фолликула и овуляции.
Построение графика базальной температуры является простым способом определить овуляцию.
График базальной температуры обычно отражает выработку прогестерона – гормона, вырабатываемого яичниками после овуляции, который на протяжении 12-16 дней после овуляции подготавливает внутреннюю слизистую оболочку матки к имплантации и развитию оплодотворенной яйцеклетки.
Чтобы составить график базальной температуры, женщина должна измерять температуру в прямой кишке каждое утро в одно и то же время сразу после пробуждения и записывать показания ежедневно по датам.Признаком овуляторного цикла являются: двухфазный характер графика температуры в течение одного менструального цикла, с падением в день овуляции на 0,2-0,3оС и подъемом температуры во второй (лютеиновой) фазе цикла по сравнению с первой (фолликулиновой) на 0,5-0,6оС при длительности второй фазы не менее 12 — 14 дней.
При отсутствии овуляции график базальной температуры монофазный (без повышения температуры после овуляции).
Однако наличие двухфазного характера не является бесспорным доказательством произошедшей овуляции или выработки прогестерона, как и монофазный характер не доказывает, что овуляция отсутствует.
Многие факторы, не связанные с репродуктивным циклом, такие как простуда или усталость, могут влиять на базальную температуру.
Подтверждением овуляции является уровень прогестерона, определяемый с 19-го по 23-ий день 28-дневного менструального цикла. В нормальном менструальном цикле пик уровня прогестерона приходится примерно на 7-ой день после овуляции. Повышение концентрации прогестерона в крови позволяет установить факт овуляции. Более точно диагностировать овуляцию можно с помощью следующих методов:
- Мочевой тест на овуляцию. Этот тест определяет увеличение уровня лютеинизирующего гормона (ЛГ) в моче и помогает предсказать время овуляции.
- УЗИ-мониторинг. С помощью УЗИ врач определяет созревает ли в яичнике доминантный фолликул и происходит ли его разрыв (овуляция).
- Биопсия эндометрия позволяет определить овуляцию по изменениям эндометрия, происходящим в ответ на выработку прогестерона. Незадолго до начала менструации из матки берется небольшой кусочек эндометрия. Биопсию эндометрия обычно проводят за 1-3 дня до ожидаемой менструации, обычно на 26-ой день 28-дневного менструального цикла, когда изменения в эндометрии под воздействием прогестерона достигают своего максимума. Биопсию эндометрия можно также проводить на 12-13-ый день после пика уровня ЛГ. Состояние эндометрия является отражением функции яичников. При ановуляции обычно обнаруживают ту или иную степень гиперплазии эндометрия или полип эндометрия (разрастание эндометрия, при котором нарушается его структура, и появляются изменения в строении желез).
Методы диагностики эндокринных нарушений
- Обследование на наличие инфекций, передающихся половым путем, спермограмма мужа;
- Определение гормонов крови: ФСГ, ЛГ, пролактин, тестостерон общий (иногда – свободный), эстрадиол (Э2), прогестерон, ТТГ (Если пациентка ранее проходила лечение по поводу бесплодия, были выкидыши или медикаментозные аборты, в таком случае анализ на ТТГ перед планированием беременности по протоколу ЭКО делают одним из первых. Для благоприятного наступления беременности показатель ТТГ при ЭКО норма должна быть не более 2,5 мЕд/л.), дополнительно – Т4 св.;
- При гиперандрогении проводится диагностика происхождения андрогенов – определение надпочечниковых фракций андрогенов: дегидроэпиандростерона сульфат (ДГЭА-с), 17-гидроксипрогестерон (17-ОП) – маркер адреногенитального синдрома; андростендиона – маркер СПКЯ;
- При аменорее на фоне повышения пролактина – рентгенография черепа в боковой проекции. Проведение компьютерной или магниторезонансной томографии головного мозга для исключения микроаденомы гипофиза или контроля эффективности лечения – по показаниям;
- Консультация окулиста (определение полей зрения и исследование глазного дна) при патологии гипофиза, партериальной гипертензии, прогрессирующем ожирении или потере веса;
- При ожирении и артериальной гипертензии — гликемия натощак и/или глюкозотолерантный тест, липидограмма, определение в суточной моче 17-кортикостероида (17-КС) и 11-оксикортикостероида (11-ОКС);консультация маммолога, УЗИ молочных желез на 8-10-й день менструального цикла;
- Трансвагинальное УЗИ внутренних гениталий при подозрении на гиперплазию эндометрия на 8-10-й день менструального цикла, в остальных случаях – после 20-го дня менструального цикла;
- При первичной аменорее проводят исследование полового хроматина, при его показателях менее 10 – кариотипирование или исследование Y-хроматина;
- При гиперандрогении проводятся пробы с преднизолоном или дексаметазоном для исключения опухолевого процесса.
- При нарушениях менструального цикла (задержке, аменорее) проводится гестагеновая проба: прогестероном, дюфастоном или утрожестаном . До 2-х недель ожидают кровотечения подобного менструации. Отсутствие менструации говорит о дефиците эстрогенов в организме.
Лечение эндокринного бесплодия
При лечении эндокринного бесплодия необходимо ормализовать работу эндокринной системы — щитовидной железы и надпочечников. Лечением эндокринной патологии занимается врач эндокринолог, а также гинеколог-эндокринолог, если у женщины возникает проблема с беременностью и зачатием.
На начальных этапах лечения эндокринного бесплодия осуществляется коррекция нормальной работы всей эндокринной системы: надпочечников, щитовидной железы, проводится коррекция сахарного диабета.
Затем применяют лекарственные препараты, стимулирующие формирование фолликула и запускающие процесс овуляции. Одним из таких препаратов является Клостилбегит.
Это достаточно недорогой препарат, вызывающий увеличение выработки ФСГ гипофизом и стимулирующий овуляцию.
Если же использование этого или аналогичного ему препарата не принесло ощутимого результата в течение 6-ти циклов овуляции, то назначаются более серьезные препараты – гонадотропины.
Существуют различные типы гонадотропинов:
- человеческий менопаузальный гонадотропин (ЧМГ): меногон, менопур;
- рекомбинантный фолликулостимулирующий гормон (р-ФСГ): гонал-Ф, пурегон;
- хорионический гонадотропин человека (ХГЧ): хорагон, прегнил.
Гонадотропины стоят намного дороже, чем Кломифен цитрат или Клостилбегит, а также имеют высокий процент вероятности возникновения побочных эффектов, например, гиперстимуляция яичников. Кроме того, после их применения увеличивается риск возникновения многоплодной беременности.
Рекомбинантные препараты ФСГ синтезируют биотехнологическими методами; они обеспечивают максимальную точность введения благодаря ручке-инжектору и могут использоваться пациенткой самостоятельно. Препараты для стимуляции овуляции подбираются строго индивидуально.
Доказано, что у женщин с показаниями ФСГ свыше 25 мМЕ/мл процент зачатия очень низок даже с применением вспомогательных репродуктивных технологий. В случае, если уровень ФСГ составляет 15мМЕ/мл так же процент зачатия очень низок.
Необходимо отметить малое количество фолликулов и соответственно меньшее количество эмбрионов возможно как у женщин с высоким, так и с низким содержанием ФСГ. Благодаря исследованиям и данным статистики можно с уверенностью сказать, что женщины в возрасте более 40 лет имеют самый низкий процент вероятности зачатия с помощью ЭКО с высоким фсг.Однако многие врачи-репродуктологи основываются на разных границах норм показаний содержания фолликулостимулирующего гормона.
Вспомогательные репродуктивные технологии при бесплодии
В большинстве случаев эндокринное бесплодие у женщин излечивается с помощью простой стимуляции овуляции посредством Кломифен цитрата (Клостилбегит) или гонадотропинами. Иногда возникает уреаплазма при эко .
У 80 % пациенток, принимающих подобные препараты, происходит стимуляция овуляции, что приводит к последующему оплодотворению. Благодаря использованию этих препаратов овуляция начинает происходить регулярно.
В течение шести месяцев такого лечения у большинства пациенток, как правило, наступает беременность. Если желаемого эффекта не произошло, то рекомендуется провести лечение бесплодия методом ЭКО.
При ЭКО применяется контролируемая стимуляция суперовуляции, которая приводит к созреванию гораздо большего числа фолликулов, чем при стимуляции Кломифен цитратом. Благодаря ЭКО многие женщины с эндокринным фактором бесплодия смогли добиться беременности.
Источник: https://registr-eco.ru/temyi/besplodie/zhenskoe-besplodie/endokrinnoie-besplodie.html
Эндокринный фактор бесплодия: признаки и методы диагностики, формы и причины заболевания, современные способы лечения и последующий прогноз

У многих женщин, планирующих беременность, обнаруживается эндокринное бесплодие. Подобная патология характеризуется различными нарушениями, итогом которых становится отсутствие нормальной овуляции.
Гормональное расстройство репродуктивной функции лечится только после комплексного обследования, а также дифференциальной диагностики. Очень важно выявить первопричину гормонального расстройства. К сожалению, не все формы болезни можно вылечить.
Однако даже в случае отсутствия терапевтического эффекта от лечения, всегда помогут вспомогательные репродуктивные методики.
Эндокринное бесплодие диагностируется очень часто. По мнению многих специалистов, эта форма бесплодия является самой распространенной.
Признаки эндокринного бесплодия
Главный симптом гормонального бесплодия – отсутствие беременности на фоне регулярной половой жизни без применения контрацептивных средств на протяжении одного года. Убедиться в том, что проблема имеет именно гормональное происхождение, можно по нескольким дополнительным признакам:
- Нестабильный менструальный цикл, обильные или, наоборот, мажущие выделения.
- Выделение жидкости из молочных желез.
- Изменение тела по мужскому типу.
- Чрезмерное оволосение.
- Снижение либидо.
- Выраженные перепады настроения.
- Возникновение угревой сыпи.
Иногда при гормональном бесплодии месячные циклы не нарушаются. Женщина живет обычной жизнью, совершенно не подозревая о присутствии расстройства. Выделения при этом являются всего лишь менструальноподобным кровотечением. Чаще всего эндокринное бесплодие обнаруживается у пациенток из следующего списка:
- Достигшие 25-летнего возраста.
- Злоупотребляющие гормональными препаратами.
- Принимающие алкоголь и наркотические средства.
- Имеющие в анамнезе опухоли половых желез.
Также бесплодие гормонального типа нередко диагностируют у женщин, которые занимаются профессиональными видами спорта, часто делают аборты, увлекаются приемом различных трав. В группу риска входят лица, рано начавшие жить половой жизнью.
Методы диагностики
Определить причины патологии возможно только после проведения разных видов диагностики.
Первый этап обследования – это сбор анамнеза, в ходе которого врач задает вопросы о самочувствии, особенностях месячного цикла, хронических заболеваниях, беременностях, перенесенных оперативных вмешательствах.
Вся эта информация нужна для того, чтобы определиться с дальнейшими действиями, понять, какие обследования необходимо выполнить.
Также во время первого визита к врачу осуществляется гинекологический осмотр в кресле, позволяющий:
- осмотреть шейку матки;
- оценить расположение и размеры репродуктивных органов;
- взять мазок для проведения анализа на микрофлору.
В основе диагностики гормонального бесплодия лежат инструментальные и аппаратные методы, а также лабораторные анализы.
Обязательно проводится ультразвуковое сканирование, с помощью которого определяется состояние матки и придатков, оценивается овариальный запас. Также УЗИ показывает особенности функционального слоя (эндометрия) в главном репродуктивном женском органе – матке.
Затем наступает очередь сдачи крови для исследования на гормоны. Ультразвуковая диагностика позволяет определить, в какой именно день необходимо осуществлять сбор биоматериала. Кровь для анализа на гормоны сдают из вены. Чтобы выяснить, насколько хорошо яичники выполняют свои функции, и наступает ли овуляция, проводятся анализы на:
- Гормоны щитовидной железы.
- Эстрадиол.
- Фолликулостимулирующий гормон.
- Лютеотропин.
- Прогестерон.
- Тестостерон.
- Пролактин.
- ДГЭАС.
Дополнительные диагностические методики, позволяющие наиболее точно установить природу возникновения бесплодия:
- Магнитно-резонансная томография.
- Лапароскопия.
- Компьютерная томография.
- Рентгенография черепа.
- Биопсия функционального маточного слоя.
Формы и причины эндокринного бесплодия
Гормональное бесплодие провоцируется нарушениями деятельности нервной системы, иммунной, эндокринной, гипоталамо-гипофизарной.
Беременность не может наступить вследствие отклонений в функционировании желез внутренней секреции. Не исключены комплексные расстройства.
Дело в том, что сбои в работе одного органа неминуемо влекут за собой проблемы в деятельности другого. В результате возникают гормональные сбои.
Очень неблагоприятно, если нарушается работа гипоталамо-гипофизарной системы, регулирующей деятельность большинства эндокринных желез. Патологические изменения обычно возникают на фоне травм, либо формирования опухолей.Они сопутствуют повышению концентрации пролактина, вследствие чего происходит уменьшение выработки фоллитропина, стимулирующего рост граафовых пузырьков, и лютеинизирующего гормона, который способствует овуляции.
Следствием всех этих процессов становится секреторное или эндокринное бесплодие.
Эндокринное бесплодие зачастую сопровождается либо нарушениями менструального цикла, либо аменореей.
Нарушение функций яичников
Когда половые железы перестают работать как нужно, у женщины развивается эндокринное бесплодие.
При данном заболевании отмечается уменьшение производства эстрадиола, необходимого для нормальных процессов созревания яйцеклеток и для роста эндометриального маточного слоя.
При климаксе такое состояние является естественным, поскольку у женщины в связи с возрастными изменениями происходит угасание репродуктивной функции.
Когда у пациентки в яичниках присутствуют фолликулы, но отсутствует реакция на выработку гормонов, то такие яичники называют резистентными. При истощенных яичниках овариальный запас уменьшается. Объясняется это перенесенными хирургическими операциями, а также различными заболеваниями.
Синдром поликистозных яичников
СПКЯ – это довольно частая причина гормонального бесплодия. При такой патологии строение половых желез изменяется, формируется плотная капсула. Кроме того, отмечается снижение чувствительности к инсулину. Многие женщины и не подозревают о наличии у себя этой болезни. В качестве симптомов можно рассматривать длинный менструальный цикл, чрезмерное оволосение тела, ожирение и др.
Избыток пролактина
Выработка пролактина увеличивается во время грудного вскармливания. Этот гормон считается природным контрацептивом, поскольку он подавляет активность половых желез при лактации. Но его избыточная концентрация, не связанная с послеродовым периодом, провоцирует развитие эндокринного бесплодия. Гиперпролактинемия вызывает прекращение ежемесячных кровотечений, овуляция не наступает.
Недостаточный или избыточный вес
Гормональный сбой может возникнуть на фоне резкого изменения массы тела.
Внезапное похудение или, наоборот, прибавка в весе, как правило, вызывают нарушения баланса в организме. Активность половых желез восстанавливается самостоятельно, если индекс массы тела соответствует норме.
При недостатке жировой ткани или ее переизбытке снижается синтез половых гормонов. Однако нужно учитывать, что чрезмерно худым женщинам гораздо сложнее зачать, нежели страдающим ожирением.
Это следует взять на заметку любительницам строгих диет.
Дисфункция щитовидной железы
Болезни щитовидки неминуемо приводят к патологиям в половой сфере и к гормональным сбоям. Чтобы ликвидировать дисбаланс необходимо установить, в какую сторону отклоняются показатели гормонов.
В эндокринологии существует такое понятие, как гипертиреоз, характеризующийся избытком гормонов, и гипотиреоз, означающий недостаточную выработку этих веществ. Подобные нарушения отрицательно воздействуют на работу яичников, повышают секрецию пролактина.
Результатом становится либо бесплодие, либо неспособность выносить ребенка.
Прогноз после лечения
Эндокринное бесплодие в большинстве случаев хорошо лечится. По статистике восьми женщинам из десяти удается забеременеть вскоре после проведенной терапии.
Легче всего устраняются нарушения в функционировании яичников, гиперпролактинемия и отклонения, вызванные переизбытком андрогенов.
Но если беременность не наступает вследствие гипоталамо-гипофизарных расстройств, то тут все намного сложнее.
При беременности, наступившей после терапии эндокринного бесплодия, необходим тщательный врачебный контроль. У таких пациенток гормональная система в любой момент может дать сбой.Поэтому если существует угроза прерывания, либо преждевременных родов, рекомендована госпитализация. Врачи должны постоянно наблюдать за состоянием организма будущей мамы и самочувствием плода.
Во многих случаях после эндокринного бесплодия пациентки нуждаются в применении стимуляторов родовой деятельности.
Чтобы предотвратить секреторное бесплодие рекомендуется следить за здоровьем с детства. Родители должны с повышенным вниманием относиться к инфекционным и вирусным заболеваниям, своевременно принимать меры. Нужно учитывать, что к расстройству репродуктивной функции может привести даже обычная ангина в хронической форме.
Источник:
Эндокринное бесплодие
Эндокринное бесплодие – комплекс гормональных нарушений, ведущих к нерегулярности овуляции или ее отсутствию у женщин и нарушению качества спермы у мужчин. В его основе могут лежать нарушения функций щитовидной железы, половых желез, гипоталамо-гипофизарной регуляции.
Лечение эндокринного бесплодия заключается в устранении его причины, коррекции существующих нарушений и поддержании нормального гормонального фона. Нормализация нарушенных функций приводит к наступлению беременности в 70-80% случаев эндокринного бесплодия. В остальных случаях в настоящее время перспективным считается устранение эндокринного бесплодия методом ЭКО.
Эндокринное бесплодие – комплекс гормональных нарушений, ведущих к нерегулярности овуляции или ее отсутствию у женщин и нарушению качества спермы у мужчин. В его основе могут лежать нарушения функций щитовидной железы, половых желез, гипоталамо-гипофизарной регуляции.
Источник: https://cmsch71.ru/drugoe/chto-takoe-endokrinnyj-faktor-besplodiya-i-lechitsya-li-patologiya.html